BET含溴结构域和额外终端域家族蛋白
BET 属于 bromodomain 蛋白家族(溴区结构域,BRDs)中的第二类,在多种肿瘤中BET 蛋白表达上调,与细胞生长、增殖分化、凋亡坏死等多种生物学过程相关,进而参与调控肿瘤发生发展的过程。BRDs 是一类进化上高度保守的蛋白质功能结构域,能够识 别并结合组蛋白尾部的乙酰化赖氨酸残基,招募染色质调节相关蛋白、转录因子、染色质重塑因子等,从而在调控基因转录和染色质重塑中发挥重要作用,是重要的表观遗传“阅读器”。BRDs 包含 8 个亚家族,BET 是其中研究最多的。人体 BET 家族由 BRD2、BRD3、BRD4、BRDT 组成。BET 蛋白含有 2 个在序列上高度保守的 BRD 结构域,分别处于其N 端和 C 端。研究显示,BET 蛋白与组蛋白的乙酰化赖氨酸结合,从而控制 c-MYC、PIM1和 BCL-2 等促生长、抗凋亡靶基因的转录。
BET 家族在人体组织广泛表达,参与肥胖、肺纤维化、慢性阻塞性肺疾病及癫痫等众多疾病的发生和发展。例如,B 细胞淋巴瘤中 BRD2 过度表达,中线癌发病与 BRD3/BRD4的 BRD 编码区和 NUT 基因染色质易位形成 BRD-NUT 融合基因相关。在造血系统肿瘤包括急性髓系白血病、Burkitt 淋巴瘤、多发性骨髓瘤及急性淋巴白血病的模型中,通过干扰 BRD4 可以抑制 MYC 表达等。BET 抑制剂能通过特异性抑制 BET 家族蛋白的功能,调控上述恶性肿瘤相关基因的转录表达,最终抑制肿瘤生长,BRDs 已成为抗肿瘤药物研发的可能靶点之一。除此之外,该类小分子抑制剂还具有抗炎、治疗心血管疾病等作用。
资料来源:Liu Z,Wang P,Chen H,et al.Drug discovery targeting bromodomain-containing protein 4[J].J MedChem,2017,60(11):4533-4558.doi:10.1021/acs.jmedchem.6b01761
临床研究申报概况
目前,国内仅有 2 项关于 BET 靶点的临床研究,即 Zenith Epigenetics 公司的ZEN003694 联合他唑来膦治疗三阴性乳腺癌患者的Ⅱb 期研究;ZEN003694 联合恩扎卢胺治疗转移性去势抵抗性前列腺癌患者的Ⅱb 期研究。其中针对乳腺癌的研究分为 3 个部分:第 1 部分、第 2部分和扩展研究部分(分为 A、B、C 队列)。而国内的恒翼生物医药科技(上海)有限公司承接了扩展研究的 C 队列。该队列(队列 C)计划在未有 BRAC 突变且没有接受过 TROP2-ADC 治疗的晚期三阴性乳腺癌的经治患者中,评估 ZEN003694与他唑来膦联用的有效性和安全性 相关阅读:ALK抑制剂临床研究现状
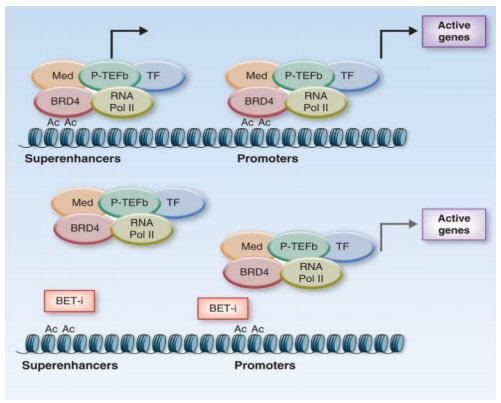
图片来源:Stathis A,Bertoni F.BET proteins as targets for anticancer treatment[J].Cancer Discov, 2018,8(1):24-36.doi:10.1158/2159-8290.CD-17-0605.
简评
正如 2021 年评述,BET 抑制剂的特异性、耐药和毒副作用等问题有待解决,虽然 2012年 GSK525762 就申报了临床试验,但经过 10 余年的研发,全球所有的 BET 抑制剂仍限于Ⅰ/Ⅱ期。2022 年似乎是个 BET 的“优势年”,Zenith Epigenetics 公司 ZEN003694 就有 4 项临床申报,除了之前所提的,还包括与 PD-1 联合治疗三阴性乳腺癌、与化疗联合治疗成年和青少年(12~17 岁)中线癌、单药治疗晚期 NSD3-扩增的肺鳞状细胞癌。期待这些早期临床试验的结果早日揭示靶向 BET 蛋白的抗肿瘤潜力。

 2023-07-04
2023-07-04 
 MCE
MCE

