AKT靶点抑制剂
1.靶点机制
经典信号通路 PAM,即磷脂酰肌醇 3-激酶(phosphoinositide 3-kinase,PI3K)-蛋白激酶 B(protein kinase B,AKT)-哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)信号通路在多种肿瘤中异常激活,参与调控肿瘤细胞增殖、分化和凋亡等生命过程,也是抗肿瘤药物研发所关注的重要通路。AKT 位于 PI3K-AKT-mTOR 通路的核心位置,具有 3 种亚型,AKT1、AKT2 和 AKT3,三者具有高度相似的结构,均由氨基末端的 PH结构域、中部的激酶结构域(ATP 结合域)和羧基末端的调节结构域组成。首先,PH 结构域 与 PIP2 及 PIP3 特异性结合,使 AKT 定位于细胞膜上;其次,激酶域将 ATP 的磷酸基团转移到底物苏氨酸上使其磷酸化,导致 AKT 具有部分活性;最后,调节域丝氨酸位点的磷酸化使 AKT 活性进一步提高,其活性结构得到进一步稳定。AKT 可通过磷酸化多种酶、激酶和转录因子等调节细胞功能,如 AKT 磷酸化 TSC1/TSC2 复合体(tuberous sclerosiscomplex)并激活 mTORC(mTOR 复合体),激活蛋白翻译,促进细胞生长。AKT 通过下游多种途径对靶蛋白进行磷酸化而参与抗凋亡;磷酸化 Bcl-2 家族成员 BAD,阻止其与Bcl-XL 结合启动凋亡。AKT 磷酸化转录因子 FOXO1,抑制其核转位而阻止其转录激活作用,AKT 激活导致 NF-κB 的抑制剂降解,增加核转录因子 NF-κB 核转位,激活其靶基因从而促进细胞迁移和侵袭等。PTEN 突变或缺失、AKT1/ AKT2/ AKT3/PIK3CA 突变或如扩增等都会引起 AKT 信号通路的过度激活,是驱动癌症生长关键途径之一,AKT 信号通路的失调在复发性卵巢癌、乳腺癌和前列腺癌等瘤种中更为普遍。
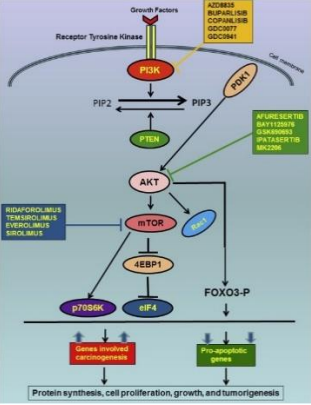
资料来源:ALZAHRANI AS. PI3K/Akt/mTOR inhibitors in cancer: At the bench and bedside[J]. Semin CancerBiol,2019,59:125-132. doi: 10.1016/j. semcancer. 2019.07.009. Epub 2019 Jul 16. PMID: 31323288.2.中国临床研究申报现状
2. 中国临床研究申报现状
针对 AKT 通路,虽然临床研究已进行多年,但至今国内外尚没有产品获批上市。最早进入Ⅲ期试验的是罗氏旗下基因泰克与 Array BioPharma 公司(已于 2019 年 7 月 30 日被辉瑞公司收购)合作研发的 pan-AKT 抑制剂帕他色替(Ipatasertib)和阿斯利康公司的卡匹色替(Capivasertib, AZD5363)。目前,AKT 抑制剂在国内申请和进行的临床研究有10 项进入Ⅲ期阶段,其中主要为国际多中心临床研究,包括评估 Capivasertib+氟维司群对比安慰剂+氟维司群治疗局部晚期或转移性乳腺癌的疗效和安全性研究;在局部晚期或转移性三阴性乳腺癌中 Capivasertib+紫杉醇对比安慰剂+紫杉醇作为一线治疗的研究;Capivasertib+阿比特龙用于治疗 PTEN 缺失的转移性激素敏感性前列腺癌的研究;比较Ipatasertib/安慰剂治疗转移性去势抵抗性前列腺癌的研究;Afuresertib 联合紫杉醇对比紫杉醇单药治疗铂类耐药卵巢癌的有效性和安全性研究;评价恩扎妥林(Enzastaurin)联合R-CHOP 对比 R-CHOP 在携带 DGM1 的初治高危弥漫性大 B 细胞淋巴瘤中的有效性和安全性研究; 在新诊断为胶质母细胞瘤并且全新生物标记物 DGM1 阳性患者中评估Enzastaurin 联合替莫唑胺同步放化疗加辅助化疗方案的研究等……
还有 5 项处于Ⅰ-Ⅱ期的临床研究,包括阿氟色替(Afuresertib)联合紫杉醇对比紫杉醇单药治疗铂类耐药卵巢癌的有效性和安全性的Ⅱ期研究;评价 LAE005+Afuresertib+白蛋白紫杉醇在晚期实体瘤中的Ⅰ期剂量递增研究及 LAE005+Afuresertib+白蛋白紫杉醇三联或者LAE005+白蛋白紫杉醇二联或者 Afuresertib+白蛋白紫杉醇二联方案治疗局部晚期或转移性三阴性乳腺癌的安全性和有效性的Ⅱ期研究;评价 Ipatasertib 在局部晚期或转移性实体瘤中国患者中的药代动力学研究,Capivasertib 用于治疗晚期实体瘤以及 APG-2449 在晚期实体瘤患者中的Ⅰ期临床研究。推荐阅读:AKT激酶抑制剂
值得注意的是,目前 Ipatasertib 联合化疗一线用于 HR 阳性/三阴性乳腺癌的两项Ⅲ期研究已经终止,终止原因与未达到预期的数据有关。AKT 抑制剂在临床研究中仍面临诸多挑战,包括药物为多靶点抑制缺少精准选择、生物利用度低、可能产生严重的不良反应、有效性不足、治疗窗口狭窄以及需要探索更为合适的给药间隔和频次等问题,未来需要进一步改善和提升这类药物的应用。
3.简评
AKT 是 PAM 信号通路的重要成员,对 AKT 的抑制可能发挥重要的抗肿瘤作用机制。目前临床研究结果提示存在 PIK3CA/AKT1/PTEN 基因突变或缺失的患者应用 AKT 抑制剂治疗可能存在获益,AKT 抑制剂具有广阔的研发和应用前景,可能成为抗肿瘤治疗的一个热门靶点。但是,AKT 抑制剂的作用机制较为复杂,影响因素众多,目前尚无该类药物获批上市,未来的研究方向在于提高激酶选择性、降低给药剂量、扩大治疗窗口,以期发现疗效更好、更安全的临床药物,探索高效和选择性好的 AKT 抑制剂是未来重要的研究方向。

 2023-06-30
2023-06-30 
 MCE
MCE

