WHO盘点十个最具潜力的小分子
8 月初,世界卫生组织(WHO)更新了第二季度的药物收录情况。众所周知,药物研发是一个漫长的周期,从成千上万个候选分子中,历经 3-5 年的临床前体内外实验筛选,最终能推进临床研究的少之又少。顺利推进临床阶段,是药物获得批准并进入市场的重要里程碑。
在这篇文章中,小 M 将结合公开资料,带大家盘一盘已快人一步进入临床试验的十个小分子药物。

01: Irpagratinib
■ 原研公司:和誉生物医药
■ 适应症:肝细胞癌(HCC)
■ 临床阶段:Ⅱ 期
Irpagratinib (ABSK011) 是一种新型、高选择性的小分子 FGFR4 抑制剂。
在临床前研究中,ABSK-011 的靶点蛋白 IC50<10 nM,相对于其他 FGFR 激酶具有至少 50 倍的选择性。口服 ABSK-011 强烈抑制皮下异种移植肿瘤的生长并诱导 FGFR4 活性依赖的消退。
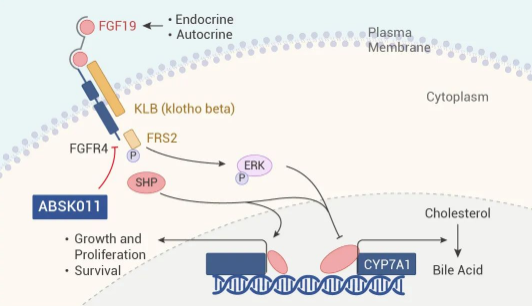
图 1. ABSK011 作用机制。
公开资料表明,ABSK-011 正在进行一项临床 Ⅱ 期研究,旨在评估其联合 Atilizumab 在晚期或不可切除 HCC 患者中的安全性和耐受性。
此外,一项 ABSK-011 作为单药治疗用于晚期 HCC 患者的临床 Ⅰ 期试验同时进行,主要评估口服 ABSK-011 的推荐扩展剂量和安全性。
02: Vorbipiprant
■ 原研公司:Rottapharm
■ 适应症:结直肠癌
■ 临床阶段:Ⅱ 期
Vorbipiprant (CR6086) 是一种新型、有效、选择性、口服的小分子前列腺素 EP4 受体拮抗剂,具有免疫调节特性。
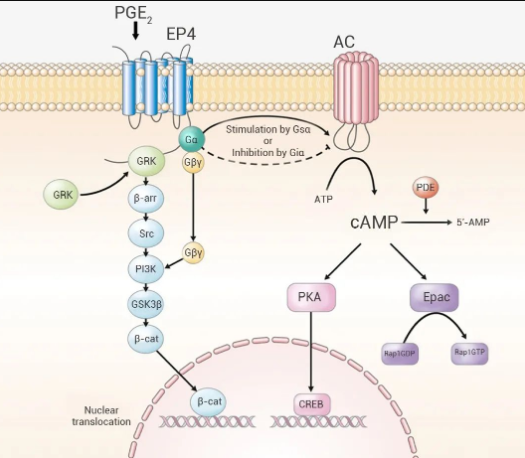
图 2. EP4 受体拮抗剂作用机制。
公开资料表明,一项 CR6086 与 Balstilimab (AGEN2034) 联合治疗难治性转移性结直肠癌的 Ⅰ/Ⅱ 期临床试验正在进行。
此外,还在进行一项 Ⅱ 期试验,旨在评估口服 CR6086 以 30、90 或 180 mg 的剂量与 Methotrexate 联合治疗类风湿关节炎患者的功效、安全性和药代动力学。
03: Glecirasib
■ 原研公司:加科思药业
■ 适应症:晚期实体瘤
■ 临床阶段:Ⅰ/Ⅱ 期
Glecirasib (JAB-21822)是一种强效的、不可逆的 KRASG12C 抑制剂,通过共价结合于 KRASG12C 的 12 位突变的半胱氨酸残基上,使 KRASG12C 锁定在非活化状态,从而阻断 KRAS 依赖的信号转导,抑制肿瘤细胞的增殖,并诱导细胞凋亡。Glecirasib 是潜在的“Best-in-class”分子。
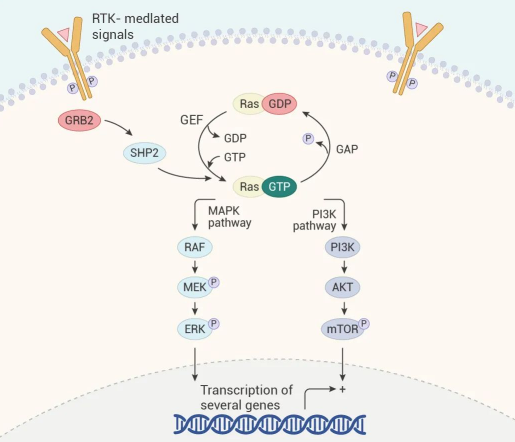
图 3. KRASG12C 抑制剂作用机制。
公开资料表明,JAB-21822 正在进行一项用于 KRAS p.G12c 突变晚期实体瘤中 Ⅰ/Ⅱ 期试验,旨在评估安全性、耐受性、药代动力学和抗肿瘤活性。
此外,JAB-21822 还进行了多项 Ⅰ/Ⅱ 期临床试验,用于非小细胞肺癌、晚期结直肠癌、阑尾癌、胰腺导管癌等适应症研究。
04: Bocodepsin
■ 原研公司:Onkure
■ 适应症:晚期实体瘤;黑色素瘤
■ 临床阶段:Ⅰ/Ⅱ 期
Bocodepsin (OKI-179) 作为核心管线,是一种新型口服生物可利用的 I 类选择性 HDAC 抑制剂。OKI-179 在临床前癌症模型中显示出抗肿瘤活性,具有良好的药代动力学特征和靶向药效作用。

图 4. HDAC 抑制剂抗肿瘤机制。
据公开资料,OKI-179 联合 Binimetinib 用于治疗 RAS 通路激活突变的晚期实体瘤患者和晚期 NRAS 突变黑色素瘤患者的Ⅰ/Ⅱ 期研究正在进行,旨在探索 OKI-179 的最佳剂量。
此外,一项 OKI-179 作为单药治疗晚期实体瘤患者的 Ⅰ 期研究已经完成。
05: Lixumistat
■ 原研公司:ImmunoMet Therapeutics
■ 适应症:晚期实体瘤
■ 临床阶段:Ⅰ 期
Lixumistat (IM156) 是一种蛋白质复合物 1 (PC1) 抑制剂,靶向线粒体中的氧化磷酸化 (OxPhos) 途径,并减少目标癌细胞和纤维化中的异常细胞生长。
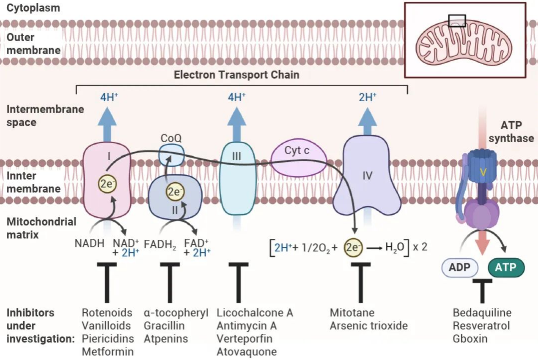
图 5. OxPhos 抑制剂作用机理。
据悉,Lixumistat (IM156) 的第一例人体试验在 M.D.安德森癌症中心进行,旨在评估 IM156 联合 Gemcitabine 和白蛋白结合型紫杉醇对胰腺癌患者的治疗效果。
此外,一项 IM156 作为单药用于晚期实体瘤和淋巴瘤患者的 Ⅰ 期临床研究已经完成,旨在评估安全性、耐受性和初步疗效。

01: Frunexian
■ 原研公司:eXIthera Pharmaceuticals
■ 适应症:血小板减少症和新冠肺炎
■ 临床阶段:Ⅱ 期
Frunexian (EP-7041) 对靶标具有高度选择性,抑制人 FXIa 的 IC50 为 7.1 nM。临床前体内研究表明,EP-7041 能够抑制血栓形成,同时最大限度地减少不必要的出血风险。
图 6. Frunexian 的 3D 结构。
公开资料表明,EP-7041 的一项 Ⅱ 期临床研究正在进行,用于在重症监护机构中治疗的 COVID-19 综合征患者的血栓预防,这是 EP-7041 的首次人体研究。
此外,EP-7041 用于关节置换术的一项临床Ⅰ期研究已完成。
02: Mosnodenvir
■ 原研公司:Janssen Pharmaceutica NV
■ 适应症:登革热
■ 临床阶段:Ⅰ 期
Mosnodenvir (JNJ-1802) 是一种泛血清型登革热直接抗病毒小分子,该分子具有皮摩尔至纳摩尔泛血清型体外效力,并在小鼠和非人灵长类动物模型中显示出体内效力。
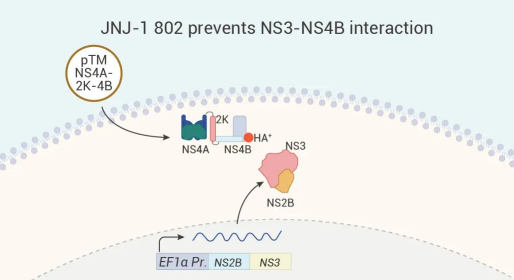
图 7. JNJ-1802 作用机理。
据文献报告,JNJ-1802 的首次人体研究主要目标包括调查健康参与者在禁食条件下单次或多次口服剂量后 JNJ-1802 的安全性和耐受性。次要研究目标是调查健康受试者在禁食条件下单次和多次口服剂量后 JNJ-1802 的药代动力学 (PK)。
03: Sutidiazine
■ 原研公司:Zydus Lifesciences Limited
■ 适应症:疟疾
■ 临床阶段:Ⅰ 期
疟疾是由疟原虫属原生动物寄生虫引起的,死亡率和发病率很高。Sutidiazine(Zy-19489)是一种新型三氨基嘧啶抗疟候选药物。
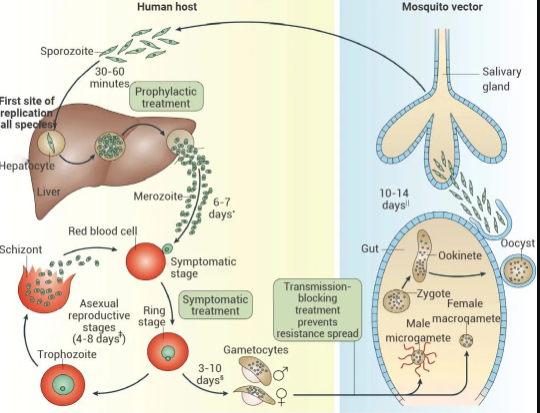
图 8. 疟虫生命周期理。
据悉,Zy-19489 通过口服途径给药,一项临床 Ⅰ 期试验已完成,旨在研究健康成人受试者的安全性、耐受性和药代动力学。
此外,一项与 Ferroquine (FQ) 组合给药的 Ⅰ 期临床试验正在进行,用于成人无症状恶性疟原虫携带者。

01: Perfluorohexyloctane
■ 原研公司:恒瑞医药
■ 适应症:干眼症
■ 临床阶段:3 期
Perfluorohexyloctane (NOV03;SHR8058) 是一种研究性、新型、单一实体、无水、不含防腐剂的滴眼剂,由 100% 全氟己基辛烷组成,可以快速在眼表面迅速扩散,形成稳定锁水层。
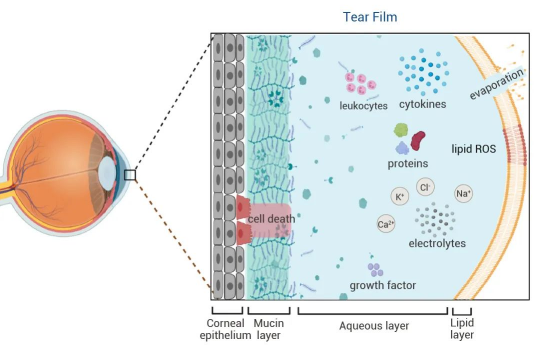
图 9. 眼表与泪膜示意图理。
公开资料显示,一项用于伴有睑板腺功能障碍的干眼病的 Ⅲ 期临床试验正在进行,并在初步的临床数据统计中,显示 NOV03 达到了两个疗效终点
02: Bemfivastatin
■ 原研公司:Furiex Pharmaceuticals
■ 适应症:高胆固醇血症
■ 临床阶段:Ⅱ 期
Bemfivastatin (PPD 10558) 作为具有口服活性的降脂 3-羟基-3-甲基戊二酰辅酶 A (HMG-CoA) 还原酶抑制剂,是一种具有增强肝脏提取功能的他汀类药物,正在开发用于治疗因他汀类药物相关而无法耐受他汀类药物的患者的高胆固醇血症肌痛
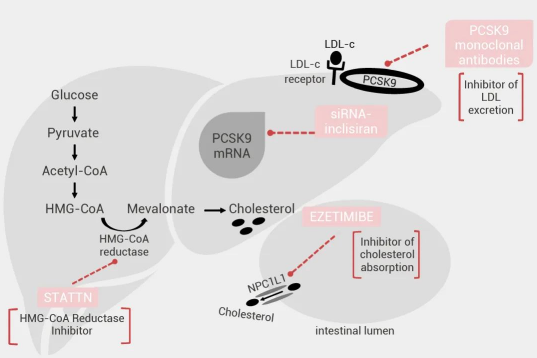
图 10. HMG-CoA 还原酶抑制剂降脂机制理
公开资料表明,PPD 10558 正在进行一项双盲、随机、安慰剂对照和主动对照对照 Ⅱb 期临床研究,旨在评估其与 Atorvastatin 在原发性高胆固醇血症 Fredrickson Ⅱa 或 Ⅱb 患者中的他汀类药物相关肌痛发生率、血脂影响以及安全性和耐受性

 2023-09-07
2023-09-07 
 MCE
MCE

