肿瘤免疫大新闻-HLA-E新的免疫检查点
肿瘤免疫大新闻!血液循环肿瘤细胞 (CTCs) 中现身新的免疫检查点 – HLA-E
初绽头角,免疫检查点
免疫监视学说认为免疫系统就像一支 “作战优良” 的部队一般,能够持续地监视体内出现的异常细胞,识别并摧毁它们。同样地,免疫系统可通过癌症免疫周期对抗杀死部分肿瘤细胞。可肿瘤细胞似乎有 “免死金牌” 一般,总神奇般 “死灰复燃”,人们对此很是困惑。直到 2006 年,Allison 提出免疫检查点,指程序性死亡受体及其配体,存在于免疫系统中,担负着上调或下调免疫系统信号的作用
简单来说,凡是可以影响免疫反应的重要靶点,都属于免疫检查点。最家喻户晓的免疫检查点便是 2018 年荣获诺贝尔奖的 PD-1 和 CTLA-4,其具有免疫抑制功能,随后肿瘤免疫治疗开始进入广大群众的视野。这不,研究人员又发现了 HLA-E 这一新的免疫检查点,让我们来一探究竟~
新的突破, HLA-E
看到下面这张图,是否又重新唤起了你儿时的记忆,NO,NO,NO,这可是 Cancer Cell 的期刊封面。近期,四川大学华西医院团队发表题为 “Immune checkpoint HLA-E: CD94-NKG2A mediates evasion of circulating tumor cells from NK cell surveillance” 的封面研究论文

Cancer Cell 封面(图片来源:Cancer Cell 期刊官网)
对于肿瘤细胞与不同类型的免疫细胞之间的免疫检查点分子对及 ICBs 的研究,大多聚焦于实体肿瘤原发病灶或转移灶中,对 CTCs 中肿瘤细胞的免疫监视探索很少关注。在这篇文章中,该团队发现了循环肿瘤细胞 (CTC) 与 NK 细胞间的一种新的免疫检查点-- HLA-E,阐述了 CTC 通过免疫检查点分子对 HLA-E: CD94-NKG2A 逃避 NK 细胞监视的新机制。作者巧妙地选取了西游记作为封面素材,将 CTC 喻为各路伪装的妖精,通过扮弱等 “绿茶” 手段骗取唐三藏 (血小板) 的信任,并误导猪八戒 (HLA-E) 来保护自己,阻止孙悟空 (NKs) 对妖精 (CTC) 的攻击。形象生动地循解释了 CTCs 与 NK 细胞之间的相互作用。
■ 移动的 "种子"
循环肿瘤细胞 CTC
1869 年,Ashworth 首次提出循环肿瘤细胞 (Circulating tumor cells, CTCs) 的概念,目前是指存在于外周血中的各类肿瘤细胞。血液循环是肿瘤从原发病灶向远处器官扩散的主要途径。CTC 就像一粒 “种子”,通过血液循环,经侵袭、内渗、循环、外渗和定殖5个步骤,最终发展成为恶性肿瘤 (图 1)。
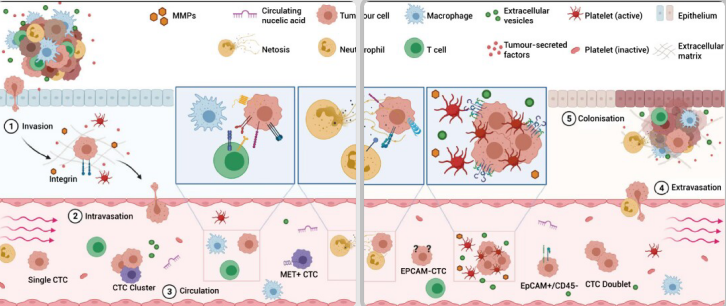
图 1. 血液传播过程中 CTC-血液相互作用示意图
■ 发现及验证
CTC 中新的免疫检查点分子对 HLA-E: CD94-NKG2A
为研究 CTCs 的相关转移机制,采集了胰腺导管腺癌患者的原发性肿瘤、肝转移灶以及肝门静脉 (hepatic portal vein, HPV) 中的血液进行活检,并利用单细胞测序技术 (scRNA-seq) 等技术,分析其转录组学特征和基因表达差异 (图 2A)。结果显示,血液循环中观察到 CTCs 和 NK 细胞之间存在主要相互作用,其中 HLA-E 和 CD94-NKG2 在 CTC 和 NK 细胞之间具有最强烈的免疫相互作用 (图 2B)。
进一步的研究发现,大多数 NK 细胞都含有这种免疫抑制受体 NKG2A,且 CTC 中 HLA-E 的表达水平高于实体病变肿瘤细胞中的表达水平 (图 2C-E)。因此,血液中 NKG2A 和 HLA-E 之间上调的相互作用可能是由 HLA-E 分子水平的增加驱动的。
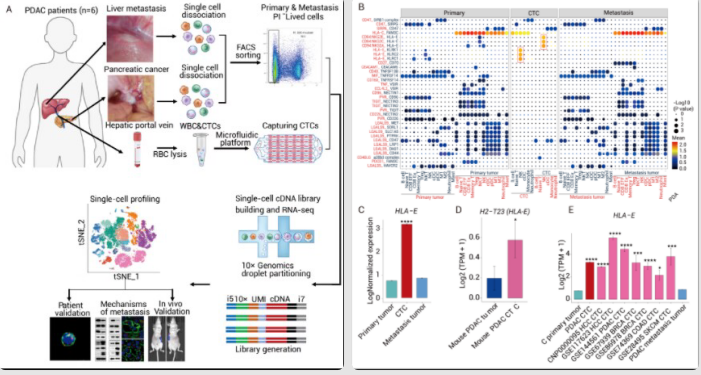
图 2. HLA-E: CD94-NKG2A 免疫检查点分子对的发现
A: 机制研究方案;B: 不同来源肿瘤细胞与 NK 细胞间的免疫检查点分子对;C-E: HLA-E 在不同来源肿瘤细胞上的表达。
随后,为验证 CTC 中 HLA-E 的免疫检查点功能,在体外进行了 NK 细胞毒性实验,在体内构建尾静脉小鼠模型来模拟 CTC 介导的转移,通过使用特异性抗体 Monalizumab 阻断 NKG2A 或敲低 HLA-E 来中断免疫检查点。体内外分析表明,CTC 和 NK 细胞通过免疫检查点分子对 HLA-E: CD94-NKG2A 相互作用。通过阻断 NKG2A 或敲低 HLA-E 表达来破坏这种相互作用可增强 NK 介导的体外肿瘤细胞杀伤作用,并防止体内肿瘤转移(图 3)。
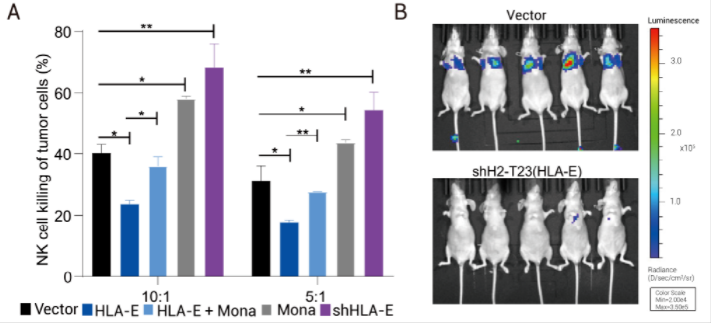
图 3. HLA-E: CD94-NKG2A 的体内外功能验证
A: 体外细胞毒性实验;B: 体内尾静脉模型中肺转移情况。
■ 机制探究
CTC 通过参与血小板来源的 RGS18 上调免疫检查点分子 HLA-E
那么 CTCs 是如何动员 HLA-E 的呢?研究人员评估了可能与 HLA-E 表达水平呈正相关的差异表达基因。观察到 RGS18 并非在原发和转移病灶的肿瘤细胞中表达,而是几乎只在 CTC 中表达。众所周知,CTC 通常被血小板覆盖,而血小板是 RGS18 蛋白的主要来源。机制研究表明,血小板源性 RGS18 通过 AKT-GSK3b-CREB 信号通路促进 HLA-E 的表达,RGS18 过表达促进胰腺肿瘤肝转移 (图 4)。

图 4. CTC 通过 HLA-E: CD94-NKG2A 逃避 NK 细胞的监视
机制探讨:
1.当向血管内灌注 CTC 时,CTC 会粘附并摄取携带 RGS18 的血小板。2.RGS18 抑制宿主细胞中 p-AKT 的活化,进而抑制 GSK3β Ser9 的磷酸化而稳定 GSK3β 蛋白。
3.GSK3β 蛋白通过 CREB1的 Ser133 位点磷酸化促进 CREB1 的核转位。
4.CREB1 与细胞核内 HLA-E 基因启动子区 SXY 位点结合,上调 CTC 表面 HLA-E 表达和易位。
5.NK 细胞表面 HLA-E 与 NK 细胞表面的 CD94-NKG2A 相互作用,激活细胞内的磷酸酶 SHP1,抑制 NK 细胞的杀伤活性。
免疫检查点阻断(ICB),大放光彩
说了这么多,免疫检查点这一 “香饽饽” 究竟有何用处呢?言至于此,便不得不提免疫检查点阻断 (Immune checkpoint blockade, ICB) 疗法,指的是基于程序性死亡受体及其配体的免疫检查点的阻断疗法,通过抑制二者的结合,释放免疫抑制调节,恢复T淋巴细胞的肿瘤特异性细胞毒性,从而提高宿主免疫系统对肿瘤细胞的攻击性[7,8]。ICB 已经为多种类型癌症的治疗带来了翻天覆地的变化,在过去的这些年,针对 PD-1 和 CTLA-4,FDA 已批准了 9 种阻断免疫检查点的单克隆抗体药物,包括 7 个 PD-1/PD-L1,2 个 CTLA-4 单抗,用于 20 多种适应症,包括转移性黑色素瘤、非小细胞肺癌、肾癌、肝细胞癌等
近年,一些新的免疫检查点分子包括 TIM-3、VISTA 和 LAG-3 等也被引入研究。例如,许多临床试验 (如 NCT03470922) 评估了不同的阻断 LAG-3 的方法联合抗 PD-1 治疗作为潜在的新型 ICBs,经过不懈努力,最终 Relatlimab 于 2022 年 3 月首次获得美国 FDA 批准治疗黑色素瘤,成为首款获批上市的抗 LAG-3 抑制剂。
大家进一步了解了肿瘤免疫中 “响当当” 的免疫检查点,并详细介绍了新的免疫检查点 -- HLA-E 及其相应机制。其次,基于免疫检查的阻断疗法给肿瘤免疫之路带来的曙光,针对经典免疫检查点的药物已获批上市,多种新型免疫检查点百花齐放,共同对抗肿瘤这个“大魔头”。
相关产品
Monalizumab
Monalizumab 是一种靶向自然杀伤细胞群 2A (NKG2A) 的免疫检查点抑制剂。Monalizumab 是一种人源化抗 NKG2A 的单克隆抗体,可增加 IFN-γ 产生,从而促进自然杀伤细胞功能。Monalizumab 可用于头颈部鳞状细胞癌 (HNSCC) 的研究。
BMS-1166
BMS-1166 是一种有效的 PD-1/PD-L1 免疫检查点抑制剂。BMS-1166 诱导 PD-L1 二聚化并阻断其与 PD-1 的相互作用,IC50 为 1.4 nM。BMS-1166 拮抗 PD-1/PD-L1 免疫检查点对 T 细胞活化的抑制作用。
Tuvonralimab
Tuvonralimab (PSB-205; QL1706) 是一种双重免疫检查点阻断剂,包含有抗 PD-1 IgG4 和抗 CTLA-4 IgG1 抗体、Iparomlimab 和 Tuvonralimab。
CA-170
CA-170 是一种口服的 VISTA 和 PD-L1 双重抑制剂。CA-170 对 PD-L1/L2 和 VISTA 抑制的 T 细胞的增殖和效应因子功能具有有效的拯救作用,选择性优于其他免疫检查点蛋白以及广泛的受体和酶。
BMS-37
BMS-37 是一种 PD-1/PD-L1 免疫检查点抑制剂。BMS-37 可作为 PD-L1 配体合成 PROTAC 分子。

 2023-04-14
2023-04-14 
 MCE小分子
MCE小分子

