单细胞蛋白免疫印迹
Western blotting 是绝大多数实验都会用到的一门实验技术了。从蛋白样品的制备到显影,步骤大家都已经烂熟于心。但是,萌 Cece 今天要跟大家要分享不一样的蛋白免疫印迹: Single-Cell Western Blotting。
Single-Cell Western Blotting (scWestern) 是基于 Western blotting 的单细胞免疫印迹技术,可用来检测复杂细胞群体中细胞间不同蛋白的表达。目前 scWestern 不像传统 Western blotting (WB) 这般普及,但是随着生物学单细胞基因组学 (单细胞全基因组测序和以单细胞和微量细胞为材料的全基因组范围内的基因功能研究) 的发展,作为单细胞蛋白质组进行定性定量分析的有用工具,scWestern 未来可期。
传统 Western blotting 与 scWestern 的区别
与传统的 WB 印迹相比, scWestern 实现了在单细胞水平上检测蛋白质表达变化的检测,并且可以精确量化由外界刺激引起的单个细胞的蛋白水平上的变化,整个流程需要时间约 4 小时
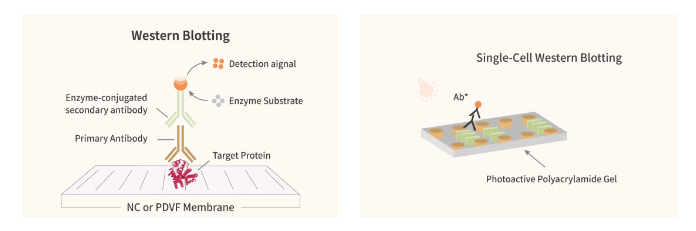
图 1. 传统 WB 与 scWestern 的区别
传统的 WB,提取的蛋白通过 SDS 变性凝胶电泳迁移之后,转移到易于在短时间内捕捉和保存蛋白的 NC 膜或者 PDVF 膜 (图 1a)。而 scWestern 实验整个过程都是具有光敏聚丙烯酰胺凝胶薄膜的显微镜载玻片 (Microscope slide) 上完成。这个载玻片上有可以固定单个细胞的凝胶槽矩阵,该阵列由上千个微孔整齐排列组成,每个微孔实质上都是一个微型的反应器 (图 1b)。
(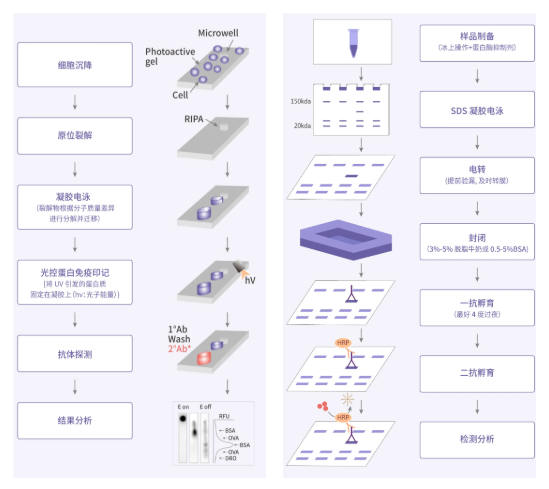

图 2. scWestern (左) 与传统 WB (右) 实验流程
将细胞通过重力沉降到 PA 凝胶微孔中,在孔中被充分裂解 (RIPA)。根据分子量大小电泳分离蛋白,这些蛋白通过微孔壁扩散到周围的 PA 凝胶。
使用紫外线照射将蛋白质固定在凝胶内,甲基丙烯酰胺的二苯甲酮共单体交联到 PA 凝胶中,与迁移的蛋白质形成共价键 (这一步替代了传统 Western blot 中繁琐的转膜实验)。一抗和二抗孵育以检测目的蛋白靶点。
scWestern 检测单细胞中目的蛋白的动态表达
scWestern 技术不仅利用传统 WB 技术的抗原抗体高特异性结合,还可以在单细胞水平报告目标分子的质量,量化目标蛋白的具体变化。
NSCs 是一种多能干细胞, 具有不断增殖和自我更新的能力, 还可以具有多分化的特征。在 2014 年,Alex J. Hughes 等在 Nature Method 发表的题为 "Single-cell western blotting" 的研究成果中,研究者采用 scWestern 技术追踪了大鼠神经干细胞 (NSC) 被诱导培养时,从成熟状态向其他细胞分化的过程。
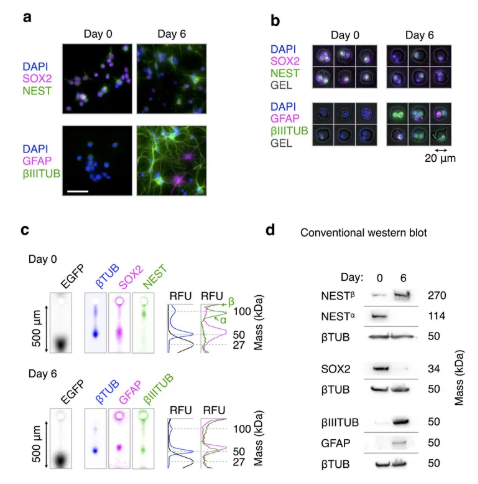
图 3. NSC分化的异质性分析
a-b: ICC 检测 NSC 分化 c: scWestern 追踪 NSC 分化时标记物的变化 d: 传统 WB。Alexa Fluor 488: Nest 和 GFAP 二抗标记; Alexa Fluor 647: Sox2和 GFAP 二抗标记 [2]
将 NSCs 将大鼠 NSC 在含 0.5 ng/mL FGF-2,1 ?M 维甲酸和 1% FBS 的 DMEM-F12-N2 培养基中诱导分化 0-6 天。检测其从不成熟状态 (标记物: SOX2+, nestin 和 NEST+) 向星形胶质细胞 (标记物: 胶质原纤维酸性蛋白 GFAP+) 和神经元细胞 (标记物: βIII-tubulin, βIIITUB+) 分化的过程。
如图 3 所示,利用细胞免疫荧光 (ICC) 检测 0-6 天培养基中被诱导的 NSC 分化 (图 3a-b),ICC 可以确认 NSC 向不同的细胞分化,但不能检测出其分化的具体类型。scWestern (图 3c) 可以检测出单个细胞中不同蛋白的具体大小,SOX2: 43.3 ± 1.9 kDa; βIIITUB: 47.2 ± 0.7 kDa; GFAP: 54.0 ± 1.0 kDa (RFU 曲线的峰的位置可以区分蛋白质的分子量)。scWestern 还可以具体分辨出 NSC 分化过程中 NEST 的 2 个亚型,NESTα (95.7±3.5 kDa) 和 NESTβ (microwell 边缘附近),NESTβ 在培养的 0-6 天表达量无太大变化,但是 NESTα 在表达细胞间和分化期间表达不定且大幅下调 (图 3c: RFU 曲线下的面积可统计为蛋白的表达量)
传统的 WB (图 3d) 也能检测出总蛋白中不同的大小的两个 NEST 亚型 (NESTα, NESTβ) 但是不能检测到单个细胞间蛋白表达的特异性。
四唑修饰的新型光敏感性丙烯酰胺凝胶的性能检测
通过上述介绍,我们得知 scWestern 的整个进程在开放式的微孔阵列芯片上,因此这一芯片的分辨率以及高固定效率,是后续拿到精确实验数据的决定因素。
近日,上海交通大学丁显廷教授团队在 Advanced Functional Materials 杂志上发表的相关论文,报道了四唑修饰的新型光敏感性丙烯酰胺凝胶 (mPyTC-modified polyacrylamide gel, MMP gel) 与未修饰的凝胶相比,具有更高分辨率与蛋白固定效率。

MMP 凝胶的性能在不同药物处理的 GES-1/MGC803 细胞系中 P-糖蛋白 (P-gp) 表达的细胞间变化中得到了证明。P-gp: ATP 结合盒转运蛋白超家族的成员外排蛋白,与化疗耐药性相关,研究 P-gp 表达在细胞间差异有助于说明耐药性的潜在机制。
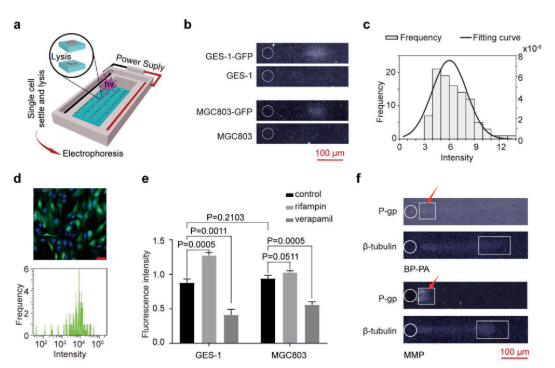
图 4. MMP 凝胶性能的检测[4]
同时使用流式和免疫荧光法与 scWestern 结果进行了对比。常规免疫荧光成像和流式细胞仪 (图 4d) 中产生的荧光密度与 scWestern 的 GFP 荧光蛋白的频率分布相似 (图 4c),上图 4a-d 的结果表明在改良的 MMP 凝胶上,紫外线诱导的光捕获对蛋白无有害影响。
为了进一步确认已开发的 MMP 凝胶检测目标蛋白质的能力,应用 scWestern 研究 GES-1/MGC803 细胞系对 P-gp 诱导剂 (Rifampicin) 或抑制剂 (Verapamil) 的反应中的细胞间异质性。如图 4f 所示: 传统的 PA 凝胶,Verapamil 治疗组中 P-gp 蛋白的荧光信号大部分被光敏凝胶的背景荧光所掩盖,但是 MMP 凝胶中则清晰可见 (图中箭头指出)。这表明了,在很短的时间 (60s) 的长波紫外线照射下,改良的凝胶可以更有效地捕获凝胶中电泳分离的蛋白。
scWestern 整合传统的 WB,使用紫外线激发激活并且固定蛋白质于凝胶内 (替代传统 WB 中繁琐的转膜实验),不仅实现了抗原抗体的高特异性结合,还实现了短时间内高通量平行分析多个单细胞的多种蛋白的表达水平,便于研究复杂细胞群体。scWestern 在药物筛选、信号通路研究等方面的应用有很大的潜力。

 2020-06-03
2020-06-03 
 MCE小分子
MCE小分子
